常见益生菌对婴幼儿健康影响的研究进展
程 斌,秦 晰,王锡青,王玉树,宋 飞*
(圣元营养食品有限公司,山东青岛 266500)
摘 要:近几年,非处方益生菌在全球范围内的消费量持续增加,已成为全球最常见的食品补充剂之一。酸奶、奶酪、冰激凌、营养棒、早餐麦片以及婴儿配方奶粉中均添加了益生菌。2021国家卫生健康委公布的《可用于婴幼儿食品的菌种名单》中,有13种益生菌可应用于婴幼儿食品(NCFM仅应用于1岁以上儿童)。本文主要选择5种典型的益生菌,汇总近几年有关动物双歧杆菌(,Bb-12)、乳双歧杆菌(,Bi-07,HN019)、鼠李糖乳杆菌( GG,LGG)和短双歧杆菌(,M-16V)在婴幼儿胃肠道功能、免疫功能和肠道菌群方面的临床研究进展,同时对益生菌的安全性、应用局限性和前景进行讨论。
关键词:益生菌;婴幼儿肠道;免疫健康
中国营养学会益生菌益生元与健康分会于2019年发布了《中国营养学会益生菌与健康专家共识》,对益生菌进行定义:益生菌是活的微生物,当摄入充足的数量时,对宿主产生健康益处。益生菌在生命早期定植于肠道,有助于建立人体肠道黏膜屏障,促进免疫功能的成熟和预防原肠道病原体的感染。在一项针对婴儿肠道微生物的调查中发现,母乳喂养的婴儿肠道菌群富含大量的益生菌,致病菌较少,这被认为是母乳喂养婴儿的感染性腹泻和过敏性疾病发病率较低的原因之一。因此,婴幼儿配方奶粉企业在婴幼儿配方奶粉的生产过程中添加益生菌,旨在模仿母乳控制婴幼儿肠道内有益菌和有害菌的含量,帮助婴幼儿建立良好的肠道微生态。
益生菌在各个健康领域发挥着作用,其中胃肠道健康和免疫功能是两个主要研究领域。本文主要针对《可用于婴幼儿食品的菌种名单》中的5种典型的益生菌,对其特性、安全性以及胃肠道和免疫功能相关的临床研究数据进行综述。
1 益生菌特性
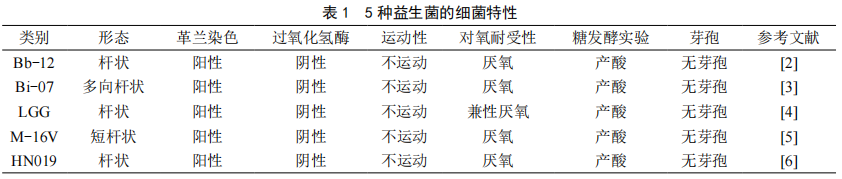
目前,国内外常用的益生菌多为乳酸菌,包括双歧杆菌、乳酸杆菌和球菌等。在我国,可应用于婴幼儿食品的益生菌只有双歧杆菌属和乳酸杆菌属。双歧杆菌属是革兰阳性、无芽孢、无运动性、过氧化氢酶阴性的厌氧杆状细菌,其最佳生长pH值为6~7,环境pH低于5.0或高于8.5几乎不生长,其最佳生长温度是37~41 ℃,其中,43~45 ℃生长最快,低于25 ℃则不生长。目前双歧杆菌约有30多种,动物双歧杆菌(Bb-12)、乳双歧杆菌(Bi-07、HN019)、短双歧杆菌(M-16V)均属于双歧杆菌属。鼠李糖乳杆菌(LGG)属于乳杆菌属,是革兰阳性、无芽孢、不运动、产酸、过氧化氢酶阴性的兼性厌氧杆状细菌,其最佳生长pH为6.8,适宜温度为30~40 ℃,37 ℃生长最优。
益生菌经人体从口腔摄入后,须经过胃到达肠道才能产生作用。因此益生菌必须承受宿主上消化道的不利条件,对胃酸和胆汁有良好的耐受性才能在下消化道保持活性和增殖能力。STASIAK[1]的一项实验研究中发现,双歧杆菌和乳杆菌可以在的模拟胃液(pH=4~5)中及胆汁盐(1%~3%)中显著生长。
2 安全性
益生菌Bb-12、Bi-07、LGG、M-16V和HN019均具有良好的安全性评价,其安全性均获得了美国食药局的GRAS认证,同时也被欧盟食品安全局列入安全性合理推定列表。在我国,Bb-12、Bi-07、LGG和HN019于2011年11月,M-16V于2016年6月被批准应用于婴幼儿食品。DIDARI的一篇系统综述中,充分阐明了双歧杆菌属和乳杆菌属的安全性,该文认为益生菌在正常使用情况下不会对机体产生任何有害作用,但重症监护室的危重病人和危重患儿及免疫功能严重低下的患者仍须谨慎使用。目前,市场上已有众多企业将益生菌作为营养强化剂添加到婴幼儿配方奶粉中,使成分更接近母乳,临床上尚未有相关不良反应事件的报道。
3 对婴幼儿胃肠道功能的影响
3.1 减轻婴儿腹泻
婴儿腹泻较为常见,通常为症状较轻的自限性疾病,一般不会有任何显著的长期后遗症。目前,益生菌在预防和治疗儿童腹泻方面的得到了广泛的研究,CHEN选择194名1~3岁儿童随机接受Bi-07(1×1010 CFU/g)和安慰剂,发现与安慰剂组相比,接受Bi-07干预的儿童腹泻症状较轻,腹泻时间平均缩短22.5 h(P<0.05),住院时间平均缩短了1.2 d(P<0.05),儿童的腹泻症状有明显改善。CHOURAQUI的一项随机对照试验选择90名8个月以下健康婴儿,随机分配接受含Bb-12(1.5×106 CFU/g)的配方奶粉或常规奶粉,发现接受Bb-12的婴儿中有28.3%发生急性腹泻,而安慰剂组为38.6%,Bb-12组发生腹泻的天数和腹泻概率均明显降低。LI的一篇Meta分析中表明,儿童早期服用高剂量LGG(≥1010 CFU/g)可以减少儿童腹泻的持续时间和每日大便次数,对腹泻的预防有良好作用。HEMALATHA的一项随机对照试验选择379名2~5岁儿童随机接受Lpc-37(2×109 CFU/d)、HN019(5×109 CFU/d)和安慰剂,发现HN019可以显著降低雨季期间儿童腹泻和发烧的发病率。这4项研究表明,益生菌制剂治疗儿童急性腹泻的疗效与细菌的个别菌株有关,Bi-07、HN019、LGG和Bb-12对婴儿腹泻有良好的保护作用。
3.2 调节肠道菌群
婴儿出生后第一年的微生物组成通常以低物种多样性和高不稳定性为特征,较易发生菌群失调引发自身免疫性疾病和慢性炎症性疾病。母乳喂养婴儿的胃肠道中,双歧杆菌数量占主导地位,被认为是婴儿肠道菌群的关键组成,在维持婴儿肠道菌群方面起重要作用。对于早期无法喂养母乳的婴儿,可以在婴儿配方奶粉中添加益生菌,提高婴儿的肠道中双歧杆菌的数量,使婴儿肠道菌群的组成更接近母乳喂养婴儿。BETTLER的一项研究选择243名12~36个月的健康幼儿随机接受Bi-07(2.6×109 CFU/d)和安慰剂,发现接受Bi-07的婴儿粪便中乳双歧杆菌含量更高(=0.01),梭菌的含量较低(<0.001)。OSWARI选择160名2~6周的儿童随机接受含HN019的配方奶粉和母乳喂养,该研究发现,益生菌组的婴儿肠道菌群与母乳喂养的婴儿基本相似,双歧杆菌在肠道微生物中占据主导地位。KOSUWON的一项研究选择129名1~3岁儿童,随机分配接受含M-16V(1×108 CFU/d)的合生元,该研究发现,M-16可以显著提高婴儿肠道中双歧杆菌的数量。这3项研究表明,Bi-07、HN019和M-16V均可以提高双歧杆菌的数量,调节婴儿肠道菌群,使肠道微生物的组成与母乳喂养的婴儿更接近。
早产儿、低出生体重儿、剖宫产儿以及接受抗生素治疗的婴儿与自然正常分娩的足月儿相比,肠道微生态更加脆弱,需要通过调节肠道菌群提高免疫力,增强婴儿体质。HUI的一项随机对照研究发现,给早产儿补充Bb-12(2×108 CFU/d)和LGG(2×109 CFU/d)可以调节早产儿肠道菌群,抑制潜在病原菌的定植。HORIGOME在医院选择22名低出生体重婴儿随机接受M-16V(1×109 CFU/d)和安慰剂。研究发现,与对照组相比,经M-16V干预的低出生体重儿粪便样本中双歧杆菌检出率高达83.3%,放线菌的丰度显著较高(<0.01),变形菌的丰度显著较低(<0.000 1),且益生菌组M-16V菌株和固有双歧杆菌的水平均显着高于对照组。由此可见,M-16V可以在大多数低出生体重儿肠道中定植并提高肠道内双歧杆菌水平。
3.3 早产儿坏死性小肠结肠炎
新生儿坏死性小肠结肠炎(Necrotizing Enterocolitis of Newborn,NEC)是由于肠黏膜遭到损伤而引起肠上皮细胞缺血缺氧而导致的小肠和结肠部分或广泛性环伺的消化系统疾病。NEC是早产儿最常见和最具有破坏性的疾病之一,多表现为腹胀、呕吐、便血等,具有发病急、进展快,且患儿的预后状态差的特点。根据美国和加拿大的新生儿网络数据库发现,在出生体重在500~150 0 g的婴儿中,该疾病的平均患病率为7%,死亡率在20%~30%。有研究认为,新生儿粪便中的短链脂肪酸与肠道感染和NEC之间存在明显的相关性。短链脂肪酸为结肠细胞提供能量,刺激大肠吸收钠和水,而过度生产的短链脂肪酸(丁酸)会导致早产儿肠黏膜损伤,并可能导致早产儿NEC的发展。有研究使用短双歧杆菌M-16V和Bi-07改善婴儿的肠道菌群,预防早产儿NEC。BENOR[7]的一项试验选择58名极低出生体重儿随机接受Bi-07(2×1010 CFU/d)或安慰剂,该研究发现,NEC的总发病率为12%,益生菌组婴儿的发病率为4%,而安慰剂组发病率为18.2%,败血症发病率和死亡率两组较为相似。BEGHETTI[8]的一项Meta分析中,选择了31项研究进行亚组分析,发现Bb-12可以明显降低早产儿NEC发病风险(95%CI)=0.03(0.00~0.21)。MEYER的一项研究选择452 9名低出生体重儿随机接受LGG
(6×109 CFU/d)干预,发现益生菌组NEC的发病率为1.6%,对照组为2.7%,且益生菌组晚发型败血症的发病率明显降低(<0.01)。YAMASHIRO的一项随机对照研究发现,接受M-16V(1×109 CFU/d)的极低出生体重儿NEC发病率和全因感染率显著降低。该研究者还发现,M-16V可以减少婴儿发热频率和抗生素的使用,减轻癌症儿童化疗所引起的黏膜炎。这4项研究表明,LGG、Bb-12、Bi-07和M-16V均可以降低低出生体重儿NEC的发病率,Bb-12和Bi-07对败血症发病率和死亡率无明显影响,LGG可以降低晚发型败血症的发病率。
4 对婴幼儿免疫系统的影响
4.1 降低特应性皮炎发病率
特应性皮炎(Atopic Dermatitis,AD),也称特应性湿疹,是一种慢性炎症性皮肤病,其特点是强烈的瘙痒、反复发作并造成皮肤损伤。近几十年来,AD的患病率在世界范围内迅速增加,多发生于婴幼儿,患病率约为10%~20%,严重影响儿童及其家庭的生活质量。目前,越来越多的证据表明,肠道菌群在过敏性疾病的发生发展中起着非常重要的作用。许多研究关注在生命早期使用益生菌补充剂预防特应性疾病。GØBEL的一项研究选择50名平均年龄为18个月的AD患儿随机接受Bi-07和安慰剂,发现服用Bi-07的患儿AD的严重程度显著降低,同时INF-γ和IL-10水平显著降低。DOTTERUD一项研究中选择415名儿童随机接受益生菌牛奶(LGG+Bb-12,5×109 CFU/d)和安慰剂。该研究结果显示,与安慰剂组相比,益生菌组AD累积发病率的OR值为0.51,P=0.013;哮喘的OR值为0.68,P=0.437;过敏性鼻结膜炎的OR值为1.52,P=0.254,表明益生菌降低AD的发病率,对机体具有保护作用,但对哮喘和过敏性鼻结膜炎无明显效果。ENOMOTO研究的一项研究选择130名孕妇在产前1个月至产后6个月服用M-16V(1×1010 CFU/d),并在婴儿第4、10、18个月时观察过敏症状的发展,发现益生菌组的婴儿在前18个月发生AD的风险显著降低(10个月,OR=0.231;18个月,OR=0.304),表明产前产后补充M-16V有效预防AD的发生。这3项研究结果表明Bi-07、LGG、Bb-12和M-16V对AD患儿有明显的保护作用。
4.2 改善牛奶过敏
牛乳蛋白过敏(Cow’s Milk Allergy,CMA)是儿童常见的一种疾病,出生后一年的发病率大约在2%~7.5%,CMA在母乳喂养的婴儿中发病率为0.5%,是3岁以下儿童中最为常见的食物过敏。目前,唯一被证实的治疗方法是从饮食中消除牛乳蛋白,因此会建议对牛乳过敏的婴儿饮用水解配方奶粉。但有众多研究发现肠道菌群与牛乳过敏有一定的关联,可以通过补充益生菌调整肠道菌群,以改善婴儿牛乳过敏。BASTURK[9]选择100名平均年龄为0~12个月的CMA儿童,随机接受含或不含LGG(1×109 CFU/d)的无奶饮食治疗,该研究发现在益生菌组患儿血便、腹泻、躁动、腹胀症状均有改善(P<0.001),腹痛(P=0.325)、便秘(P=0.917)等症状无明显改善。该研究表明LGG可以改善CMA儿童的部分胃肠道症状,具有良好的保护作用。
JEROEN选择119名CMA婴儿随机接受含有Bb-12(1×107 CFU/d)的深度水解蛋白配方奶粉12个月,发现婴儿在第6个月和第12个月时,益生菌组和对照组CMA的累积耐受性百分率相似,因此在深度水解蛋白配方中补充Bb-12并不会增强CMA患儿对牛奶的耐受性。CHATCHATEE的一项随机对照研究发现,CMA患儿补充含M-16V(1.4×109 CFU/d)氨基酸配方奶粉后,在第12和24个月分别有45%和64%的患儿对牛奶产生耐受性,普通氨基酸配方奶粉分别为52%和59%,两组之间并无显著性差异。这两项研究表明,Bb-12和M-16V均不会提高CMA患儿对牛奶的耐受性。
4.3 增强儿童的免疫功能
宿主微生物群与免疫系统之间的平衡关系对于抵御病原体攻击和预防异常炎症至关重要。研究表明,微生物群可以为宿主提供多种功能,包括增强肠道上皮屏障,维持免疫稳态和免疫反应,保护宿主免受病原体攻击等。PIERRO选择203名健康儿童,随机接受Bb-12(1×1010 CFU/d)和安慰剂,发现与对照组相比,接受Bb-12的婴儿急性胃肠炎的发病率和持续时间分别降低了82%和45%,上呼吸道感染的发病率和持续时间分别降低了84%和50%,且益生菌组的儿童唾液中IgA水平增加了3倍。LUOTO的一项随机对照实验,选择94名早产儿(出生后3~60 d),随机分配为益生菌组(LGG;1×109 CFU/d,1~30 d;2×109 CFU/d,31~60 d)和安慰剂组,并在实验开始的第1、2、4、6和12个月进行随访。该研究结果显示,与安慰剂组相比,LGG(RR=0.49,P=0.051)能够显著降低婴儿呼吸道感染的发生率。SAZAWAL选择624名1~3岁儿童随机接受含HN019(1.9×107 CFU/d)的牛奶和安慰剂并随访1年,该研究发现与对照组相比,HN019可以使痢疾的发病率降低21%,肺炎的发病率降低24%,急性下呼吸道感染的发病率降低35%。这3项研究表明,Bb-12、HN019和LGG可以提高婴幼儿的免疫功能并减少疾病发生。
DEMURI的一项研究中选择21名儿童每天服用5×109 CFU的益生菌(Bi-07),连续服用30 d,发现在补充益生菌后,MPIF-1的水平显著下降,免疫标记物水平发生变化。在结合预期炎症/抗炎作用进行分析时,发现IL-10升高,而MPIF-1、IL-8、干扰素-γ诱导蛋白10、MIP-3α和E-选择素等5种免疫因子发生下降。该研究表明,Bi-07是安全的,可以显著调节外周血单核细胞对R848的免疫应答以及MPIF-1和MIP-3α等免疫因子的水平,这一作用可能是益生菌预防病毒性上呼吸道感染的重要机制。LEYER选择326名儿童(3~5岁)随机食用NCFM(1010 CFU/d;N=110)、NCFM+Bi-07(1010 CFU/d)和安慰剂,持续干预6个月。该研究结果显示,与对照组相比,NCFM组和混合益生菌组儿童的发热率分别减少53%和72.7%,咳嗽分别较少41.4%和62.1%,流涕分别减少28.2%和58.8%,发热、咳嗽和流涕持续时间分别减少32%和48%。抗生素使用率分别减少68.4%和84.2%,因病缺课天数分别减少31.8%和27.7%。这3项研究表明,儿童补充Bi-07可以安全有效的减少发热、流涕、咳嗽的发生和持续时间,提高免疫力,预防病毒性上呼吸道感染,并且能够有效减少抗生素的使用率和因病缺课天数,对儿童的预防保健有有益作用。
5 结论
众多研究表明,Bi-07、HN019、Bb-12和LGG不仅可以调节肠道微生态,降低腹泻的发生率,还可以提高婴幼儿的免疫功能,为婴儿提供良好的保健作用。M-16V可以促进早产儿肠道微生物的定植和成熟,并防止NEC和特应性皮炎的发展。尽管支持使用M-16V的机制尚不完善,但M-16V可以调节肠道微生物群和炎症反应,降低危及生命的疾病和免疫介导性疾病的风险,这一点已十分明确。综上所述,这5种益生菌已成为对婴幼儿健康有积极影响的益生菌菌株,并具有可靠的安全记录,有望成为预防婴儿(特别是脆弱的早产儿群体)不良健康相关疾病的重要菌株。
目前,益生菌的临床研究更多的集中于婴幼儿的预防保健作用,尚未有报道表明益生菌在治疗疾病尤其是重大疾病方面的治疗作用,SCHNADOWER[10]的一项随机对照研究使用LGG对患有急性肠胃炎的儿童进行干预,发现与对照组相比,患儿并无良好预后。因此,益生菌可以作为营养强化剂应用于婴幼儿食品方面,但在婴幼儿的疾病治疗方面应全面考虑风险收益比并谨慎使用。未来,我们仍需要对益生菌的商业潜力和医学价值进行进一步的研究。
参考文献
[1]STASIAK-RÓAŃSKA L,BERTHOLD-PLUTA A,PLUTA A S,et al.Effect of simulated gastrointestinal tract conditions on survivability of probiotic bacteria present in commercial preparations[J].International Journal of Environmental Research and Public Health,2021,18(3):1108.
[2]张琳,徐加英,石羽杰,等.双歧杆菌BB-12及其免疫调节功能的研究进展[J].上海预防医学,2020,32(7):
600-605.
[3]TURCK D,CASTENMILLER J,HENAUW S D,et al. subsp. lactis Bi-07 contributes to increasing lactose digestion: evaluation of a health claim pursuant to article 13(5) of regulation (EC) No 1924/2006[J].EFSA Journal,2020,18(7):e06198.
[4]唐昱婷,汤加勇,赵华.鼠李糖乳杆菌对肠道屏障功能的影响机制研究进展[J].四川农业大学学报,2021,39(4):427-432.
[5]WONG C B,IWABUCHI N,XIAO J Z.Exploring the science behind bifidobacterium breve m-16v in infant health[J].Nutrients,2019,11(8):1724.
[6]ALI M A,HUI W,LIN G,et al.Development of a standard curve to account for viable loads of subsp. lactis HN019 Using RNA by Real-Time PCR[J].Journal of AOAC International,2019,102(2):532-538.
[7]BENOR S,MAROM R,BEN TOV A,et al.Probiotic supplementation in mothers of very low birth weight infants[J].American Journal of Perinatology,2014,31(6):497-504.
[8]BEGHETTI I,PANIZZA D,LENZI J,et al.Probiotics for preventing necrotizing enterocolitis in preterm infants: a network meta-analysis[J].Nutrients,2021,13(1):152.
[9]BASTURK A,ISIK I,ATALAY A,et al.Investigation of the efficacy of GG in infants with cow’s milk protein allergy: a randomised double-blind placebo-controlled trial[J].Probiotics and Antimicrob Proteins,2020,12(1):138-143.
[10]SCHNADOWER D,TARR P I,CASPER T C,et al. GG versus placebo for acute gastroenteritis in children[J].The New England Journal of Medicine,2018,379(21):2002-2014.

相关热词搜索:
[责任编辑:]

 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!






参与评论