实时直接分析质谱法快速检测保健酒中非法添加的12种PDE5抑制剂
齐春艳,黎欣欣,张 静,雷 毅
(广东省食品检验所(广东省酒类检测中心),广东广州 510000)
摘要:目的:建立一种实时直接分析离子源(Direct analysis in real time,DART)结合四极杆/静电轨道离子阱高分辨质谱法(quadrupole/orbitrap high resolution mass spectrometry,Q-Orbitrap HRMS)快速筛查保健酒中非法添加的12种PDE5抑制剂。方法:样品经80%乙腈水超声提取,过0.22 µm微孔滤膜后用DART-Q-Orbitrap HRMS联用仪测定。DART离子源的电离模式为正模式,样品传输速率为0.20 mm/s,离子化温度为400 ℃,栅极电压为400 V。Q-Orbitrap HRMS扫描模式为全扫描/数据依赖性二级扫描(Full MS/ddMS2)。结果:在全扫描模式下测定目标化合物的一级精密质量数,与理论精密质量数相比,相对质量偏差小于1.89 ppm,可实现精准定性;同时采集二级质谱信息,进一步提高定性准确性。该方法检出限范围为0.03~2.50 mg/kg,满足筛查要求。结论:该方法具有分析速度快,定性准确,环境友好等优势,可作为保健酒中非法添加的12种PDE5抑制剂的快速筛查和精准定性检测方法。
关键词:质谱法;保健酒;PED5抑制剂;非法添加
保健酒是以白酒或其他酒类为酒基,选择有治疗作用和滋补性能的中药或药食同源物质如人参、鹿茸、海马、海参等,通过浸泡、浸渍、蒸馏等加工手段制成的饮料酒,具有滋补健体、缓解疲劳、行气活血等保健作用[1-2]。面对巨大的市场需求和利益诱惑,一些不法商家为凸显产品功能,吸引消费者,在其产品中非法加入西地那非、伐地那非、育亨宾等PDE5抑制剂(5型磷酸二酯酶抑制剂),达到获取暴利的目的[3]。由于非法添加存在随意性大,剂量不明确等问题,消费者若长期、超量食用可能会引起心律失常、心肌梗塞、高血压等不良反应,甚至威胁生命安全[4]。
目前,PDE5抑制剂的检测方法主要有胶体金免疫层析法(GICA)、薄层色谱法(TLC)、拉曼光谱法、近红外光谱法(NIRS)、液相色谱法(LC)和液相色谱串联质谱法等(LC-MS/MS)。其中,GICA法、TLC法、拉曼光谱法、NIRS法往往存在灵敏度低、选择性差、假阳性等问题[5]。LC法和LC-MS/MS法因其高灵敏度和高选择性,是目前常用的检测方法。这些方法传统检测方法虽然前处理比较简单,但是往往存在分离分析时间长,有机试剂消耗量大,环境污染大等缺点。
DART-Q-Orbitrap HRMS法是结合了敞开式常压电离源和高分辨质谱仪两者优势的一种检测技术。采用DART离子源进行检测时,待测样品无需冗长的色谱分离过程,分析速度快,可实现实时定性分析。Q-Orbitrap HRMS结合了四级杆的高选择性和离子阱的高灵敏度、高分辨率的优势,可实现目标物的准确定性。
本研究采用DART-Q-Orbitrap HRMS技术,建立了一种保健酒中12种PDE5抑制剂快速筛查与精准定性的检测方法。该方法具有分析速度快,有机试剂用量少、绿色环保等优势。此外,通过一级全扫描获得12种PDE5抑制剂的精确质量数,根据各目标物的提取离子图进行初步定性,同时结合数据依赖性二级扫描模式获得12种PDE5抑制剂的二级特征质谱图,实现目标化合物的精准定性。本方法能够快速、准确、高效地完成保健酒中12种PDE5抑制剂的快速筛查和精准定性,为维护保健酒行业的健康发展和保障我国食品安全提供技术支持。
1 材料与方法
1.1 材料与试剂
西地那非、红地那非、伪伐地那非、氨基他达拉非、育亨宾(纯度均≥99.0%,中国食品药品检定研究院);羟基豪莫西地那非、那红地那非、硫代西地那非(纯度均≥99.3%,加拿大TLC标准品公司);硫代艾地那非、伐地那非(纯度均≥98.6%,美国Stanford Chemicals有限公司);他达拉非(纯度为99.2%,德国Dr.Ehrenstorfer GmbH公司);去甲基他达拉非(纯度为99.3%,北京坛墨质检科技股份有限公司);乙腈(色谱纯,德国Merck公司);试验用水为一级水(自制);GHP针式过滤器(0.22 µm,美国波尔有限公司)。
1.2 仪器与设备
DART实时直接分析离子源(美国Ion Sense公司);Thermo Q-Exactive Orbitrap超高分辨质谱仪(美国Thermo Fisher公司);电子分析天平(MS105DU、PL602E,瑞士Mettler Toledo公司);移液器(1~10 µL、10~100 µL、100~1 000 µL,1.0~10 mL,德国Eppendorf公司);EOAA-HM-01多管涡旋混合器(上海安谱实验科技股份有限公司);KQ-500DE数控超声波清洗器(东莞科桥超声波设备有限公司);Milli-Q超纯水系统(美国Millipore公司)。
1.3 试验方法
1.3.1 标准溶液配制
分别称取各标准品10 mg(精确至0.01 mg)于10 mL容量瓶,用乙腈溶解并定容至刻度,得浓度为1.00 mg/mL的标准物质储备液。贮存于2~8 ℃冰箱中。
分别准确移取10 µL各标准物质储备液于10 mL容量瓶中,用80%乙腈水稀释并定容至刻度,得浓度为1.0 mg/L的混合标准工作溶液。
1.3.2 仪器条件
DART离子源条件设置:电离方式为正离子模式;离子化气体为氦气,压力为0.55 MPa;待机气体为氮气,压力为0.30 MPa;进样模式为12-Dip-it模式;离子源出口至质谱进口距离为2.40 cm;样品传输速率为0.20 mm/s;离子化温度为400 ℃;栅极电压为400 V。
Exactive条件设置:电离方式为正离子模式;离子传输管温度为250 ℃;扫描方式为Full MS/ddMS2;一级扫描范围:/ 100~1 000;一级扫描分辨率70 000;AGC target:1e6;Maximum IT:100 ms;二级扫描分辨率:17 500;AGC target:1e5;Maximum IT:50 ms;NCE:20 eV、40 eV、60 eV。
1.3.3 前处理条件
准确称取混匀后的保健酒样品1 g(精确至0.01 g)于50 mL容量瓶中,加适量80%乙腈水溶液,涡旋混匀,超声15 min,放冷至室温,用80%乙腈水定容至刻度,摇匀,过0.22 µm微孔滤膜,供DART-Q-Orbitrap HRMS检测。
2 结果与分析
2.1 样品传输速率
本试验将样品传输速率分别设置为0.2 mm/s、0.3 mm/s、0.4 mm/s、0.5 mm/s和0.6 mm/s,对浓度为1.0 mg/L的12种PDE5抑制剂混合标准工作溶液进行测定。样品传输速率在0.2~0.6 mm/s范围内,离子响应强度随着样品传输速率的增大逐步降低。这是因为样品传输速率越大,目标化合物与离子化气体接触越不充分,离子化效率较低,离子响应强度也随之降低。因此,综合离子响应强度、峰形等因素,最终选择样品传输速率为0.2 mm/s。
2.2 离子化温度
本试验以50 ℃为步长,在250~550 ℃范围内,对浓度为1.0 mg/L的12种PDE5抑制剂混合标准工作溶液进行测定。在250~400 ℃范围内,离子响应强度随着温度的升高而增强,当温度高于400 ℃后,离子响应强度随着离子化温度的升高而降低。因此,最终选择400 ℃作为离子化温度。
2.3 栅极电压
本试验考察栅极电压在250~500 V范围内,以50 V为步长,对浓度为1.0 mg/L的12种PDE5抑制剂混合标准工作溶液进行测定。在250~400 V范围内,离子响应强度随着栅极电压的增大而增强;当栅极电压大于400 V后,离子响应强度随着栅极电压的增大而降低。因此,最终栅极电压选择为400 V。
2.4 定性过程

LC-MS/MS法通常利用保留时间、离子对丰度比等信息进行定性,而Q-Orbitrap HRMS测得的一级精密质量数即可作为定性的依据[6]。12种PDE5抑制剂的一级精密质量数理论值与试测值之间的相对质量偏差在0.02~1.89 ppm范围内,均小于5.0 ppm,满足定性需求。本研究同时采集了二级特征碎片离子信息,通过一级质谱信息与二级特征碎片离子信息相结合的方式,实现精准定性。12种PDE5抑制剂的质谱分析参数见表1。
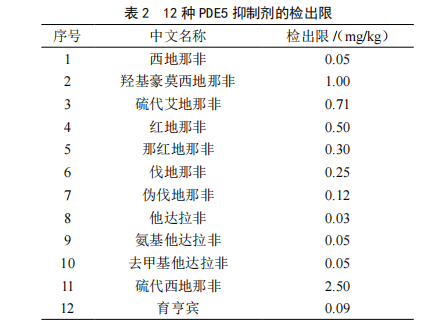
2.5 检出限
通过在空白保健酒基质中添加不同浓度水平的12种PED5抑制剂混合标准溶液,确定各个物质的检出限。如表2所示,12种PDE5抑制剂检出限在0.03~2.50 mg/kg范围内,满足筛查的需求。
2.6 市售样品的检测
采用本文建立的方法对市售的10批次保健酒样品进行检测,每个样品重复3次进样,采用一级提取离子图和一级精密质量数对样品中可能添加的12种PDE5抑制剂进行初步定性筛查,若出现可疑样品,结合二级特征碎片离子进行进一步确证。筛查结果发现1批次鹿尾巴酒为西地那非阳性样品。采用国家现行食品补充检验方法--BJS 201805 食品中那非类物质的测定(第一法)进行检测。结果表明,该批次鹿尾巴酒为西地那非阳性样品,含量为681 mg/kg。
3 结论
本研究将DART与Q-Orbitrap HRMS两者优势相结合,建立了一种保健酒中12种PDE5抑制剂快速筛查与精准定性的检测方法。该方法无需色谱分离过程,分析速度快,有机试剂消耗量少,绿色环保。此外,Q-Orbitrap HRMS通过一级全扫描获得12种PDE5抑制剂的一级精确质量数,同时以数据依赖性二级扫描模式获得的二级特征质谱信息为基础,构建了12种PDE5抑制剂质谱数据库,此数据库作为自建数据库可不断扩充,为实现保健酒中非法添加化学药物的快速筛查和精准定性提供数据支撑。本方法能够快速、准确、高效地完成保健酒中12种PDE5抑制剂的快速筛查和精准定性,为维护保健酒行业的健康发展和保障我国食品安全提供技术支持。
参考文献
[1]刘正才,陈章捷,郭菁,等.超高效液相色谱-串联质谱法同时测定保健酒中14种黄酮类成分的含量[J].食品安全质量检测学报,2020,11(7):2178-2184.
[2]王玉洁,王倩,胡正伟,等.浅析中国保健酒市场的现状及应用前景[J].农产品加工,2019(11):89-90.
[3]刘子雄,黄景辉,谭贵良,等.超高效液相色谱-串联质谱法测定保健食品中78种非法添加化学药物[J].现代食品科技,2020,36(12):283-292.
[4]孙健,胡青,张甦,等.超高效液相色谱-三重四极杆质谱法测定保健食品中30种非法添加壮阳类化合物[J].分析测试学报,2018,37(4):419-426.
[5]朱燕燕,马桂娟,龚慧.HPLC-MS/MS法同时测定保健食品中11种壮阳类非法添加[J].食品工业,2020,41(1):315-318.
[6]国家市场监督管理总局.BJS 201805食品中那非类物质的测定[EB/OL].(2018-07-17)[2021-09-24].https://www.doc88.com/p-7877817926821.html.

相关热词搜索:
[责任编辑:]

 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 挪帝克开设京东旗舰店 与京东全球购达成战略合作
挪帝克开设京东旗舰店 与京东全球购达成战略合作
 2019《食品安全导刊》杂志订阅返百元红包!
2019《食品安全导刊》杂志订阅返百元红包!
 9月大事 | 市场监管总局开展2018年全国“质量月”活动
9月大事 | 市场监管总局开展2018年全国“质量月”活动
 盒装水果省事不卫生 实验解释3大疑问
盒装水果省事不卫生 实验解释3大疑问
 使用梅特勒-托利多X光机的五大理由
使用梅特勒-托利多X光机的五大理由
 小个头 大营养 禾泱泱有机稻鸭原生小泱胚芽米 金
小个头 大营养 禾泱泱有机稻鸭原生小泱胚芽米 金
 全球食品创新平台第五期已启动,携手共创安全、健康
全球食品创新平台第五期已启动,携手共创安全、健康






参与评论