大肠菌群盲样考核结果分析
张 杨
(广元市产品质量监督检验所,四川广元 628000)
摘 要:目的:为使各微生物实验室达到比较一致的检验质量和质控水平,发现食品安全抽检工作中存在的问题,提高检验结果的准确度和可信性,参加2020年度由四川省市场监督管理局组织的盲样考核工作。方法:依据《食品安全国家标准 食品微生物学检验 大肠菌群计数》(GB 4789.3—2016)第二法大肠菌群平板计数法对盲样进行大肠菌群定量分析。结果:该盲样的大肠菌群数为4.0×104 CFU/mL,结果评价为满意。结论:此次盲样考核对微生物检验能力和检验过程各个环节质量控制的提高有重要作用。
关键词:盲样考核;大肠菌群;质量控制
大肠菌群是世界上大多数国家和组织评价食品卫生质量的重要安全性指标之一,因和肠道致病菌有密切的相关性,大肠菌群在食品微生物指标体系中占有重要地位,被称为粪便污染指示菌[1]。2020年度四川省市场监督管理局组织开展食品安全监督专项抽检,其中28批次大肠菌群不符合食品安全国家标准,主要不合格产品为瓶装饮用水、糕点、调味品、餐具等。大肠菌群超标反映出食品企业卫生状况不达标,可能与加工原料受污染、产品的灭菌不彻底、卫生操作规范执行不严格、包装材料受污染等原因有关[2]。食品微生物实验室的常规检验项目包含大肠菌群检验,是绝大部分食品都会要求检验的项目。检验大肠菌群方法有很多种,本次盲样考核要求采用平板计数法,适用于大肠菌群含量较高的食品。
1 材料与方法
1.1 盲样来源和保存
由中国检验检疫科学研究院测试评价中心下发玻璃瓶包装的冻干块状样品,样品到达实验室后,按盲样考核作业指导书要求立即放入-15 ℃以下的冰箱中保存。
1.2 培养基试剂和仪器设备
本次盲样考核中使用的结晶紫中性红胆盐琼脂(以下简称VRBA)、煌绿乳糖胆盐肉汤(以下简称BGLB)均由青岛海博生物技术有限公司提供,并进行性能试验且在有限期内,符合使用要求。
生化培养箱、电子天平、高压蒸汽灭菌锅、生物安全柜等。
1.3 方法
按照《食品安全国家标准 食品微生物学检验 大肠菌群计数》(GB 4789.3—2016)第二法大肠菌群平板计数法进行检验[3]。
1.3.1 样品制备
需要用总计40 mL灭菌生理盐水再水化,即本次冻干的样品等同于40 mL的食品样品。首先从冰箱中取出盲样使其达到室温后,将西林瓶无菌开启,立即加入4 mL灭菌生理盐水进行再水化,冻干块状样品溶解后,放入准备的无菌锥型瓶中,再反复用余下的生理盐水清洗西林瓶内壁,回收清洗液放入上述无菌锥型瓶中,此溶液为待测样品原液[4]。
1.3.2 样品稀释
用无菌吸管吸取25 mL待测样品原液,放入盛有225 mL无菌生理盐水中振摇,充分混匀,制成1︰10的样品匀液。用1 mL无菌吸管吸取1︰10样品匀液1 mL注入9 mL无菌生理盐水试管中,混合均匀,制成1︰100的样品匀液,按上述操作以此类推稀释至1︰10 000。每稀释一次,换一根无菌吸管。
2 结果与分析
2.1 平板计数
吸取1︰10~1︰10 000稀释度样品匀液1 mL于无菌平皿中,每个稀释度做2个无菌平皿,同时取1 mL无菌生理盐水加入无菌平皿中作空白对照。将平皿中倒入融化并恒温46 ℃的VRBA琼脂15~20 mL,并小心转动平皿,混合均匀,待琼脂凝固后,再加入3~4 ml VRBA覆盖平板表层,翻转后置于(36±1)℃培养24 h。结果见表1。
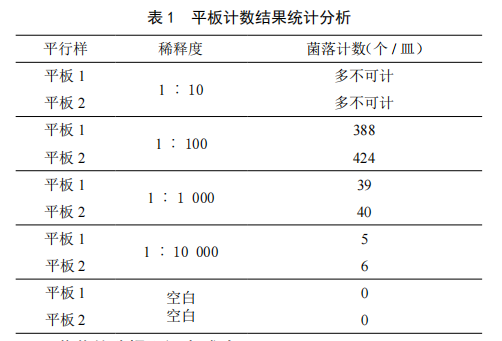
2.2 菌落的选择和证实试验
经培养后,VRBA平板上均出现0.5~3 mm紫红色周围有红色胆盐沉淀环的菌落。由表1可知,只有1︰1 000稀释度的菌落数在计数范围之内,从1:1 000稀释度的两个VRBA平板上挑取10个不同类型的典型和可疑菌落分别接种到BGLB肉汤管中,(36±1)℃培养48 h后10支BGLB肉汤管均出现产气现象。
2.3 大肠菌群平板计数的报告
该盲样的大肠菌群数为:
40×10/10×103 mL=4.0×104 CFU/mL。
2.4 项目结果评价
本次食品中大肠菌群(定量)检测项目盲样考核结果评价为满意。
3 结论与讨论
(1)参加考核前,要认真阅读盲样考核作业指导书,按其要求对待测样品进行前处理。由于食品中微生物的数量和种类会随着环境的改变而出现消长,故食品微生物盲样样品很少提供食品实物,多数为人工模拟样品的冻干粉形式出现。对于定量项目来说冻干块的样品为一个样品单元,它是一个不可分割的整体,不能仅用一部分来检验,其次样品的均匀性也会对检验结果造成直接影响,因此要在无菌条件下将样品充分混匀后随机取样。
在日常检验工作中首先需根据产品选择适当的检测方法,若食品中大肠菌群含量较低,可选择半定量计数MPN法,而大肠菌群较多的食品则可以选择定量计数平板法[5]。其次,要选择合适的稀释度,稀释度越高,检验人员的工作量越大,稀释度选择太低,平板上的菌落数又多不可计算。《食品安全国家标准 食品微生物学检验 大肠菌群计数》(GB 4789.3—2016)中要求选择2~3个适宜的连续稀释度,但作为盲样考核,为了保证数据的准确性,需要根据实际情况多选择几个稀释度,同时检验过程中尽量选取双人双平行同步检验,减少人员误差。
(2)培养基对目标微生物检出的准确性起重要作用,使用培养基时应严格按照《食品安全国家标准 食品微生物学检验 培养基和试剂的质量要求》(GB 4789.28—2013)进行制备和验证。结晶紫中性红胆盐琼脂作为选择性培养基是不需要进行灭菌的,煮沸2 min即可使用,该培养基需现配现用,不得超过3 h。在检验过程中,为防止有迁徙性细菌生长蔓延,对观察结果造成影响,必须待第一次倾注的VRBA凝固后,再将其覆盖一层,其目的是隔绝空气,降低需氧菌生长速度。
为了提高大肠菌群的检出率这就要求平时要多观察VRBA平板上大肠菌群的不同形态,并挑取菌落进行BGLB肉汤管证实试验,这样才能对大肠菌群的各种形态了然于心,防止检验工作中错检漏检。
(3)验证试验时,为了降低检验过程中的误差,挑取菌落时需注意典型菌落和可疑菌落的比例。《食品安全国家标准 食品微生物学检验 大肠菌群计数》(GB 4789.3—2016)要求选取菌落数在15~150 CFU的平板,挑取10个不同类型典型和可疑菌落,少于10个菌落的挑取全部典型和可疑菌落进行BGLB发酵验证试验,但是并未说明每个平板挑取10个还是两个平板总共挑取10个。如果平板上菌落形态单一,则两个平板总共挑取10个进行验证,若平板上菌落形态差异较大,则最好是每个平板上挑取10个菌落进行验证,并且对典型和可疑菌落按照比例挑取验证,最终计算结果时,还需要分别计算典型菌落的阳性率和可疑菌落的阳性率。
提高实验室质量控制是为了确保检验工作的准确性,为产品质量评价提供可靠的依据。积极参加盲样考核和能力验证活动,是对实验室技术能力和管理状况进行考核的方法之一,也是保证实验室资质质量的重要手段,对实验室质量控制十分重要。
参考文献
[1]雷兰兰.食品微生物能力验证的重要因素[J].现代食品,2018(12):4-6.
[2]唐轶君,张建军,李晶,等.水中铜绿假单胞菌盲样考核结果与分析[J].生物化工,2017(3):46-49
[3]中华人民共和国国家卫生和技术生育委员会.食品安全国家标准 食品微生物学检验 大肠菌群计数:GB 4789.3—2016[S].北京:中国标准出版社,2016.
[4]辛双阳,董庆林,何天文.浅析食品中大肠菌群检测能力验证的质量控制[J].食品安全导刊,2021(15):72.
[5]郭军明,孙焕芝,侯秀珍,等.对VRBA大肠菌群平板计数法的试验改进及研究[J].农业技术与装备,2021(5):28-29.

相关热词搜索:
[责任编辑:]

 挪帝克开设京东旗舰店 与京东全球购达成战略合作
挪帝克开设京东旗舰店 与京东全球购达成战略合作
 2019《食品安全导刊》杂志订阅返百元红包!
2019《食品安全导刊》杂志订阅返百元红包!
 9月大事 | 市场监管总局开展2018年全国“质量月”活动
9月大事 | 市场监管总局开展2018年全国“质量月”活动
 盒装水果省事不卫生 实验解释3大疑问
盒装水果省事不卫生 实验解释3大疑问
 “食安中国网”手机站上线通知
“食安中国网”手机站上线通知
 食安中国网关于2015年春节放假的通知
食安中国网关于2015年春节放假的通知
 小个头 大营养 禾泱泱有机稻鸭原生小泱胚芽米 金
小个头 大营养 禾泱泱有机稻鸭原生小泱胚芽米 金
 全球食品创新平台第五期已启动,携手共创安全、健康
全球食品创新平台第五期已启动,携手共创安全、健康
 食品安全新动向讲座:权威解读食品安全中的过敏原问
食品安全新动向讲座:权威解读食品安全中的过敏原问
 【采访ADM】力行不辍、多元发展,满足消费者的营养
【采访ADM】力行不辍、多元发展,满足消费者的营养
 食品掺假与成分检测网络研讨会
食品掺假与成分检测网络研讨会






参与评论