药品加强全程管 保障群众用药安
一一国家药监局局长焦红调研江苏省药品监管工作
钟卫平 滕志铭 本刊记者柴占阳
4月16日,国家药监局局长焦红一行调研江苏省药品监管工作。
国家药监局注册管理司副巡视员李芳、药审中心副主任兰奋等参加调研。
江苏省药监局局长王越陪同调研。
在江苏省食品药品监督检验研究院、省医疗器械检验所,焦红先后视察了生物技术实验室、检验技术研究中心实验室等,详细询问了实验室硬件配备、实验室管理、专业检测能力等情况。

焦红充分肯定了江苏省食品药品监督检验研究院实施内部质量管理的做法。她强调,要注重技术支撑单位能力建设,切实发挥技术机构在药品监管工作中的支撑作用,通过专业技术手段实现风险早发现、早防范。
在先声药业有限公司研发总部、正大天晴药业集团股份有限公司南京基地等实地调研中,焦红重点关注了企业创新药研发进展、“4+7”中标药品质量保障和产品供应情况。
在听取企业有关情况介绍后,她勉励企业要高度重视药品研发创新和产品质量管控,走高质量、创新发展道路,努力成为具有国际竞争力、国内示范作用的标杆企业。她强调,带量采购是国家重大改革举措,企业要牢记社会责任担当,在确保产品质量的同时,保证药品及时供应,切实使广大患者受益。

在调研座谈会上,王越汇报了江苏省级药品监管机构改革情况、针对防范化解药品安全风险所做的工作以及下一步工作打算,重点介绍了江苏省局围绕加强风险管理所做的总体安排和探索尝试。
一是在机构设置方面。将监管与审批分离,突出以监管为中心,设置药品生产、医疗器械生产、药械经营、化妆品监管处,强化监管处室风险防控职能,在稽查处加挂风险监测管控处;同时,首创在设区市设置派出检查机构,作为省药监局的重要组成部分,为深化推进风险管理提供强有力的体制保障。

二是在监管机制方面。加快完善基于风险管理的监管制度,综合 “双随机、一公开” 监管要求和药械化监管的专业性、特殊性,建立重点监管与 “双随机、一公开” 检查相结合的监管模式。组织对全省药品、医疗器械、化妆品生产企业等进行排查摸底,全面掌握企业基本信息和监管信息,建立完善监管档案。
三是在事权划分方面。明确局机关有关处室、检查分局的职责分工,厘清职责边界,严格落实监管责任。分类制定药品、医疗器械、化妆品监督检查计划,细化任务分工,原则上,省局处室主要负责高风险重点产品、重点企业的监管,检查分局主要负责其他产品和企业的日常监管。
四是在自身管理方面。要对应省局 “三定” 规定,明确机构设置基本要求和业务规范,建立局机关及检查分局质量管理体系,提升内部运行管理的规范化标准化水平。坚持问题导向,全面排查监管理念、制度、方法等方面存在的不足和漏洞,补齐短板、改进措施,持续提升风险管控能力。

在认真听取江苏省药监局有关工作汇报后,焦红高度评价了江苏省局加强检查机构建设等工作在全国的示范作用,充分肯定了江苏省局在药品监管、仿制药质量和疗效一致性评价等方面取得的成绩。
她强调,要坚决贯彻落实“四个最严” 要求,加强全程监管,切实保障群众用药安全有效。就下一步工作,焦红对江苏省局提出明确要求:
一是稳步有序推进机构改革,确保改革期间药品监管责任落实落地。要按照“不立不破”的原则,明确机构改革期间各级监管部门责任,加强对市县级监管部门的指导和督查,确保工作任务落实到位、有序衔接。
二是厚植风险管理的监管理念,深入排查、认真化解风险隐患。既要保障对疫苗企业的监督检查频次,也要提升检查效能,提高发现问题、解决问题的能力。要把通过一致性评价品种的监管摆在突出位置,杜绝降价可能引发的质量风险。

三是继续深入推进审评审批制度改革,切实发挥省药监局 “改革参与者” “企业身边人” 的作用。要鼓励企业研发创新,加强对企业的指导和培训,满足群众对创新药品的强烈需求。
四是加强技术支撑单位建设,提升技术支撑能力。要紧紧围绕中心工作,切实发挥技术机构在产品注册、审评审批制度改革、上市后监管等方面的重要作用。要加强与市场监管部门的沟通协调,统筹利用好原市县级检查力量。
五是积极参与国家药监局药品有关法律、法规、规章的制修订工作。要以国家药品监管法律、法规、规章集中修订为契机,积极参与,认真思考,把江苏在药品监管实践中的深刻体会和深入思考融入到国家局的修法工作中!

相关热词搜索:
[责任编辑:]

 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
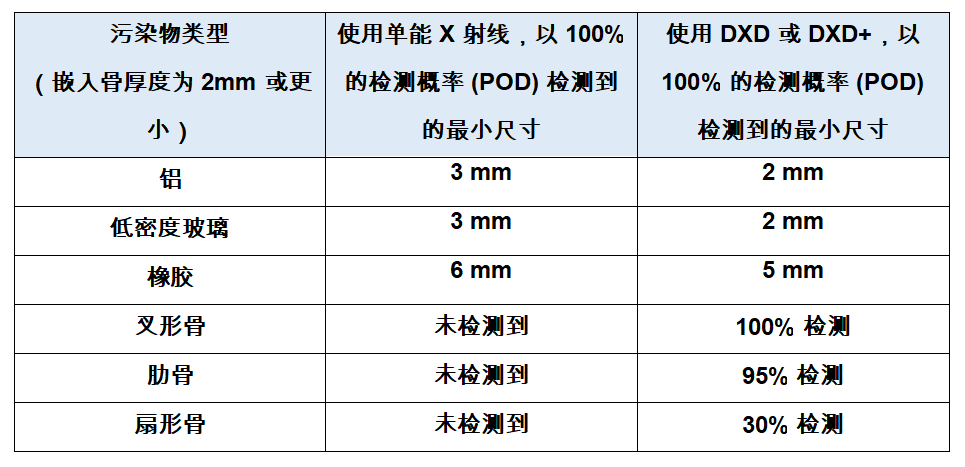 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!
 沃尔玛食品安全协作中心首次发布《愿景报告》
沃尔玛食品安全协作中心首次发布《愿景报告》






参与评论