四环素类药物时间分辨荧光层析检测试纸条的研制
□ 万宇平 崔海峰 王兆芹 宋灏 丛倩千 北京勤邦生物技术有限公司、北京市食品安全免疫快速检测工程中心
摘 要:本试验建立了一种检测四环素类药物的时间分辨荧光免疫层析技术,并在动物源性食品中对其检测性能进行了研究。实验结果显示,对猪肉、鸡肉等动物组织样品中四环素类药物的检测限为:四环素30μg/kg、金霉素60μg/kg、土霉素40μg/kg、强力霉素80μg/kg;对100ppb的磺胺二甲基嘧啶、恩诺沙星、氯霉素等药物无交叉反应,特异性较好;变异系数小于6%,精密度高;试纸条对高、低温不敏感,稳定性强。
关键词:四环素类药物 时间分辨荧光免疫层析技术 快速检测
四环素类药物(TCs)主要由放线菌属产生,是氢化骈四苯环衍生物,具有广谱高效的杀菌抗生功效,对大部分的革兰氏阴性和阳性菌及少数酵母有抑制效果,可与大多数药物或饲料添加剂混用,现已被广泛应用于畜禽养殖生产中[1]。但是,四环素类药物在使用过程中存在着长期滥用的情况,残留在动物源性食品中的四环素类药物经过人们的饮食转移到人体内,其在体内的消化分解物会抑制蛋白质的合成而导致含氮代谢物增加,从而加大肾脏的工作负担,容易引起肾小管坏死,甚至会因肾功能衰竭而死亡[2]。同时,四环素类药物在人体内的累积容易引起恶心、呕吐、食道溃疡[3]、骨生长暂时性抑制及过敏反应,肝功能障碍者甚至会出现休克、尿毒症[4]等症状,严重威胁着人们的身体健康,为此世界各国对TCs残留的检测十分关注。我国规定,牛奶中土霉素、四环素、金霉素残留限量为100μg/L;欧盟第675/92号令中初步规定,在鸡肉及牛奶中的四环素类药物含量不得超过100μg/kg,在肾脏、肝脏及鸡蛋中的含量分别不得超过600μg/kg、300μg/kg、200μg/kg;日本《肯定列表制度》规定,奶和鸡蛋中四环素类化合物的总量分别不得超过100ng/mL和400ng/mg[5]。
现阶段,国内外主要利用高效液相色谱法、毛细管电泳法、微生物法、酶联免疫法、电化学分析等对四环素类药物进行定性和定量检测[6-13]。上述各种方法曾在不同时期得到广泛应用,也各自存在着不同于其他方法的优势与劣势。具体而言,色谱法需要价格昂贵的大型仪器设备,步骤繁琐、耗时且对操作人员的专业性要求较高,不适用于基层企事业单位的大通量快速筛查检测;酶联免疫试剂盒或胶体金快速检测试纸条具有检测速度快、价格便宜、操作简单等优点,但其准确性和重复性较差,基质效应明显,无法实现定量检测,且颜色单一,背景干扰大,容易造成假阳性或假阴性的结果。因此,亟需开发一种简单快速、准确度高的检测方法——时间分辨荧光免疫层析检测方法恰好可以满足此类需求。本实验研发了一种检测四环素类药物的时间分辨荧光免疫层析试纸条,并在食源性动物食品的检测中进行了应用。
1 实验材料和方法
1.1 材料
1.1.1 实验耗材
PVC板,购于上海金标生物科技有限公司;时间分辨荧光微球,购于苏州为度生物技术有限公司;吸水垫、硝酸纤维素膜、样品垫,购于普利来基因技术公司;四环素类药物残留胶体金检测试纸条,北京勤邦生物技术有限公司自制。
1.1.2 试剂
四环素类药物、各种交叉反应药物、牛血清白蛋白、卵清蛋白,购自Sigma公司;分泌四环素类药物单克隆抗体的杂交瘤细胞株,北京勤邦生物技术有限公司制备;其他常规化学试剂均购自国药集团。
1.2 仪器与设备
时间分辨荧光免疫分析仪和旋涡混匀器,北京勤邦生物技术有限公司自有;Milli-Q Reference纯水仪,购自Millipore公司;2000SBL电子天平,购自美国setm公司;冷冻干燥机,购自Imagene公司。
1.3 试验方法
1.3.1 荧光微球标记四环素类药物单克隆抗体的制备
取市售的内部包埋荧光染料、表面修饰有羧基官能团的微球悬液100μL混悬于900μL、pH5.5~6.5、0.05mol/L的2-(N-吗啡啉)乙磺酸(MES)活化缓冲液中,于4℃下10000r/min离心10min后弃上清,重悬微球于1mL活化缓冲液中,以此法洗涤微球2次,加入适量活化剂,混匀后室温震荡活化10min。将上述混悬液于4℃下10000r/min离心10min后弃上清,重悬于pH7.5~8.5、0.05mol/L的硼酸盐偶联缓冲液中,以此法洗涤微球2次,加入10~20μL四环素类药物单克隆抗体溶液(蛋白浓度为1mg/mL),混匀后室温震荡偶联120min。获得混悬液于4℃下10000r/min离心10min后弃上清,重悬于0.1~0.4mol/L伯胺(盐酸羟胺、乙醇胺或氨基乙醇)、1%~10%BSA且pH7.4的PB封闭缓冲液中,以此法洗涤微球1次,混匀后室温震荡封闭30min,然后于4℃下10000r/min离心10min后弃上清,重悬于0.01%NaN3、0.1%BSA且pH7.4的PB贮存缓冲液中,以此法洗涤微球1次,混匀后于4℃避光保存。
1.3.2 试纸条的制备
①硝酸纤维素(NC)膜的制备
用0.05mol/L、pH7.2的PBS缓冲液将四环素类药物半抗原-卵清蛋白偶联物稀释到100μg/mL,用Isoflow点膜仪将其喷涂于NC膜上的检测区(T),喷膜量为1.0μL/cm。用0.01mol/L、pH7.4的PBS缓冲液将羊抗鼠抗体稀释到200μg/mL,用Isoflow点膜仪将其喷涂于NC膜上的质控区(C),喷膜量为1.0μL/cm。将制备好的NC膜置于37℃条件下干燥2h,备用。
②样品吸收垫的制备
将样品吸收垫用含0.5%牛血清白蛋白(体积分数)、pH7.2、0.1mol/L的磷酸盐缓冲液浸泡2h,置于37℃下烘干2h,备用。
③试纸条的组装
将样品吸收垫、硝酸纤维素膜、吸水垫从左至右依次搭接粘贴固定在底板上,样品吸收垫的末端与硝酸纤维素膜的始端相连,硝酸纤维素膜的末端与吸水垫的始端相连,样品吸收垫的始端与底板的始端对齐,吸水垫的末端与底板的末端对齐,然后用机器切成宽3.96mm的小条,装在特制的塑料制卡中,形成试纸卡。
将试纸卡与微孔试剂组装成四环素类药物时间分辨荧光免疫层析试纸条,在2~8℃下阴凉避光干燥保存,有效期为12个月。
1.3.3 样品前处理
准确称取1g±0.01g组织样品至10mL离心管中,加入3mL样本提取液,涡动2min充分混匀后,3000r/min离心5min后取上清(若上层有漂浮物则拨开取上清)待检。
1.3.4 检测过程
用微量移液器准确吸取100μL待检样品溶液于微孔中,小心抽吸至充分与微孔中试剂混匀,室温(20~25℃)作用3min;吸取孔内混合液全部量(约100μL)垂直滴加于试纸卡加样孔(S孔)中,液体流动时开始计时,室温反应5min;用时间分辨荧光免疫分析仪或紫外光下肉眼判读结果。
1.3.5 检测结果分析
阴性(-):若荧光检测仪的显示屏幕上结果显示为阴性,或紫外灯下肉眼观察T线亮度比C线亮度亮一半以上,则表示样本中不含有四环素类药物或其浓度低于检测限。
阳性(+):若荧光检测仪的显示屏幕上结果显示为阳性,或紫外灯下肉眼观察T线亮度比C线亮度暗一半以上,则表示样本中四环素类药物浓度等于或高于检测限。
无效:若质控区未检出荧光信号强度,表明操作过程不正确或试纸卡已失效。
2 结果与分析
2.1 精密度试验
向猪肉组织中分别加入1/2、1、2倍检测限浓度的四环素类药物,以未加入四环素类药物的猪肉组织为空白对照,每组检测10次,结果如图1所示。
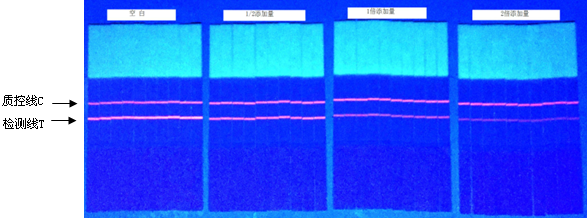
图1 试纸条精密度试验检测图
由图1可明显看出,同一添加浓度下,平行检测样的检测结果相同,同时检测线亮度保持一致。通过荧光检测仪对T、C线的亮度进行读数,计算试纸条的变异系数小于6%,说明本试验研发的四环素类药物的时间分辨荧光免疫层析快速检测试纸条检测性能稳定,精密度高。
2.2 检测限试验
向空白猪肉、鸡肉样品中分别添加四环素类药物标准品至终浓度为:四环素15、30、45、60μg/kg,金霉素30、60、90、120μg/kg,土霉素20、40、60、80μg/kg,强力霉素40、80、120、160μg/kg,分别以未添加四环素类药物的猪肉、鸡肉组织为空白对照,用时间分辨荧光免疫层析试纸条进行检测验证,检测结果如图2所示。

图2 试纸条检测限实验图
图2显示,随着四环素类药物浓度的增加,试纸条检测结果阴性越明显。当猪肉组织和鸡肉组织中四环素类药物的添加量为1倍,即四环素为30μg/kg、金霉素为60μg/kg、土霉素为40μg/kg、强力霉素为80μg/kg时,T线亮度为C线亮度的一半左右,结合读数仪的检测结果可以进一步印证,本试验研发的四环素类药物的时间分辨荧光免疫层析快速检测试纸条对四环素、金霉素、土霉素和强力霉素的检测限分别为30μg/kg、60μg/kg、40μg/kg、80μg/kg。
2.3 特异性试验
分别向猪肉组织中添加30μg/kg四环素(TC)、100μg/kg磺胺二甲基嘧啶(SM2)、恩诺沙星(ENR)、氯霉素(CAP),以未添加任何药物的猪肉组织为空白对照,每个样品做2次平行试验,检测结果如图3所示。

图3 试纸条特异性试验检测图
图3显示,当向检测样中添加30μg/kg四环素时,试纸条检测结果为阳性,而添加100μg/kg磺胺二甲基嘧啶、恩诺沙星、氯霉素等药物的检测样品检测结果均为阴性,即本试纸条对磺胺二甲基嘧啶、恩诺沙星、氯霉素等药物无交叉反应,特异性好。
2.4 稳定性试验
将试纸条分别置于4℃和37℃下14d与28d,相同情况下检测加入30μg/kg四环素的猪肉组织和鸡肉组织样品中,以未经过处理的试纸条检测值为空白对照,每个样品做3次平行试验,分别采用肉眼判断和读数仪对检测结果进行测定,用于检测四环素类药物的时间分辨荧光免疫层析试纸条稳定性,结果如表1所示。
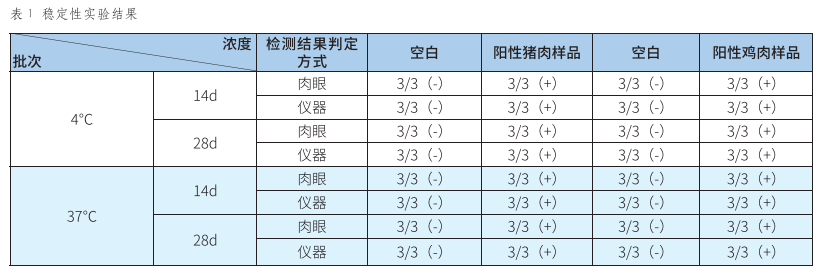
从表1可以看出,本试验研发的四环素类药物的时间分辨荧光免疫层析快速检测试纸条经高、低温处理后对四环素类药物的检测灵敏度没有发生显著变化,表明试纸条稳定性较强。
2.5 与其他检测方法的对比
分别用勤邦公司的四环素类药物检测胶体金试纸条、时间分辨荧光试纸条和仪器方法测定添加不同浓度四环素类药物的猪肉组织,仪器方法参考GB/T 21317-2007 《动物源性食品中四环素类兽药残留量检测方法 液相色谱-质谱/质谱法与高效液相色谱法》(本方法对四环素、金霉素、土霉素、强力霉素检测限均为50μg/kg),检测结果如表2所示。

表2的检测结果显示,胶体金试纸条对四环素类药物的检测限最低,时间分辨荧光试纸条次之,但均高于仪器检测法,均符合我国、欧盟和日本对四环素类药物残留的相关规定。
3 讨论
本试验成功开发了一种动物源食品中四环素类药物的时间分辨荧光免疫层析快速检测试纸条,采用本试纸条对不同动物源性食品中四环素类药物残留检测的精密度、检测限、特异性和稳定性等性能指标进行了探讨,同时将本试验研发的检测方法同已有的胶体金和仪器检测方法进行了比较,结果显示,本试验研发的试纸条检测限高于胶体金、低于仪器检测法。但是,同胶体金试纸条相比,本试验研发的四环素类药物时间分辨荧光免疫层析快速检测试纸条制备过程中需要的原材料少,尤其是对抗原和抗体的需求量远少于胶体金试纸条,制作成本低。此外,由于本试纸条采用荧光微球模式,其染料荧光猝灭大大减少,发射强而稳定,检测结果不受猪肉、鸡肉等组织检测样中杂质的影响,有效提高了检测结果的准确性和稳定性。
综上,本试验研发的四环素类药物的时间分辨荧光免疫层析快速检测试纸条可用于四环素类多种药物的同时检测,其准确性和可靠性均可满足我国、欧盟和日本对四环素类药物的检测技术的要求。同时,该方法具有检测灵敏度高、操作简便、稳定性好、生成成本低等优点,可用于不同动物食源性食品中四环素类药物的快速检测分析,应用前景广阔。
参考文献:
[1] Chopr I. Tetracycline Analogs whose Primary Target is not the Bacterial Ribosome [J]. Antimicrob Agents Chemother,1994,124(38):637-664.
[2] 俞雷.警惕四环素族药物引起的肾损害[J].医药导报,1994,7(1):39-40.
[3] 杨芰,宋金春,蔡鸿生.四环素类抗生素不良反应[J].医药导报,1994,7(1):39-40.
[4] 陈高英,杨青林,司荣君,等.四环素的不良反应及过敏反应[J].畜牧兽医科技信息,2005,6(4):53.
[5] Zhou H, Zhu T, Wang Y. The Effects of The New Pesticide Residue Standards of Japan Positive List System on Chinese Agricultual Products Export [J]. Modern Food Science And Technology,2006,12(22):197-199.
[6] 张素霞,李俊锁,钱传范.牛奶中四环素类药物多残留分析方法研究-MSPD-HPLC-UV[J].畜牧兽医学报,2002,33(1):51-54.
[7] 沈洪刚,程玲玲,方智,等.酶联免疫法快速测定猪肉中四环素族残留量[J].检验检疫科学,2000,10(2):42-43.
[8] 刘智宏,叶妮,黄耀凌,等.ELISA法测定牛奶和鸡肉中四环素类药物残留[J].中国兽药杂志,2006,40(11):1-4.
[9] 刘智宏,叶妮,郭文林,等.四环素类药物多残留酶联免疫检测方法[J].中国农业科学,2009,42(1):318-323.
[10] 刘丽,蔡志斌,张英.高效液相色谱法测定水产品中土霉素、四环素、金霉素[J].中国卫生检验杂志,2007,17(8):1405-1406.
[11] 贾薇,孙璐,史向国,等.液相色谱-质谱联用法测定牛奶中4种四环素类药物残留量[J].沈阳药科大学学报,2002,19(2):333-337.
[12] 国占宝,武玉香,田文礼,等.食品中四环素类残留的酶联免疫检测试剂盒的研制[J].食品科学,2011,32(2):333-337.
[13] 杜红鸽,郭芙蓉,陈蔷.四环素类药物残留分析方法研究紧张[J].河南畜牧兽医(综合版),2008,8(6):13.
基金项目:河北省科技计划项目资助(16275507D)。

相关热词搜索:
[责任编辑:]

 挪帝克开设京东旗舰店 与京东全球购达成战略合作
挪帝克开设京东旗舰店 与京东全球购达成战略合作
 2019《食品安全导刊》杂志订阅返百元红包!
2019《食品安全导刊》杂志订阅返百元红包!
 9月大事 | 市场监管总局开展2018年全国“质量月”活动
9月大事 | 市场监管总局开展2018年全国“质量月”活动
 盒装水果省事不卫生 实验解释3大疑问
盒装水果省事不卫生 实验解释3大疑问
 “食安中国网”手机站上线通知
“食安中国网”手机站上线通知
 食安中国网关于2015年春节放假的通知
食安中国网关于2015年春节放假的通知
 企业交流学习的桥梁 食品人技能提升的平台
企业交流学习的桥梁 食品人技能提升的平台
 探讨食品安全未来趋势 引领食品安全技术发展
探讨食品安全未来趋势 引领食品安全技术发展
 CAC (China) HACCP内审员
CAC (China) HACCP内审员
 2019《食品安全导刊》杂志订阅返百元红包!
2019《食品安全导刊》杂志订阅返百元红包!
 食品企业收到《行政处罚决定书》后应如何处理?
食品企业收到《行政处罚决定书》后应如何处理?





参与评论