关于ISO/IEC 17025:2017的解读
 讲师简介:张泽楷,NSF International中国实验室质量经理。拥有10年食品及第三方检测机构QA经验;熟悉ISO 17025、CMA、CNAS、ISO 22000、HACCP等质量管理体系,历经政府和用户审核50余次,其服务对象包括CMA、CNAS、DAKKS(德国认可委)、恒天然、家乐福、玛氏、卡夫、通用磨坊、皇家宠物Royal Canin等。
讲师简介:张泽楷,NSF International中国实验室质量经理。拥有10年食品及第三方检测机构QA经验;熟悉ISO 17025、CMA、CNAS、ISO 22000、HACCP等质量管理体系,历经政府和用户审核50余次,其服务对象包括CMA、CNAS、DAKKS(德国认可委)、恒天然、家乐福、玛氏、卡夫、通用磨坊、皇家宠物Royal Canin等。近年来由于食品安全问题频发,国家相关部门加大了对食品安全检测方面的投入,新的实验室不断涌现,传统实验室也在不断改革和创新。但是,实验室的质量管理一直是各实验室面临的共性问题,人员、设备、安全、技术、数据等的管理等都会对实验室的检测效率及质量产生直接影响。另外,标准的变化也会让实验室的管理面临一定的挑战。例如,由国际标准化组织ISO/CASCO(国际标准化组织/合格评定委员会)制定的实验室管理标准ISO 17025,其最新版本ISO/IEC 17025:2017已于2017年11月30日已正式发布,这是自2005年以来最新的一次修订。
最新版本的ISO 17025包含哪些重要内容?同之前2005年5月版本相比有什么突出变化?另外,实验室的数据应如何管理?在由《食品安全导刊》、食安中国网共同举办的“互联网+实验室标准管理体系”网络论坛中,来自NSF中国实验室的张泽楷老师分享了最新版ISO 17025:2017的变化,他从ISO 17025标准的发展历史、修订思路、修订内容等几个方面做了相应的解读。
ISO/IEC 17025标准的历史与发展
要想详尽地了解ISO/IEC 17025,就要了解其发展历程。ISO/IEC 17025最初被叫做ISO导则25,于1978年由国际实验室认可合作组织(ILAC)编写后推荐给ISO,并被ISO接受,随之被命名为《实验室技术能力评审指南》,所以ISO 17025可以说是对技术能力的评审。1982年,国际电工委员会(IEC)参与了ISO 17025的修订,文件名称改为《检测实验室基本技术要求》;1988年,导则25吸收了ISO中管理和要求的内容;1990年,ISO/IEC导则25:1990《检测和校准实验室能力的通用要求》面世。以上三版都称为导则,直至1999年被正式命名为17025,第四版的名称为ISO/IEC 17025:1999《检测和校准实验室能力的通用要求》;之后一版为2005年发布并一直沿用至2017年的ISO/IEC 17025:2005《检测和校准实验室能力的通用要求》。截至目前,最新的版本就是本次网络论坛要解读的ISO/IEC 17025:2017《检测和校准实验室能力的通用要求》。
ISO/IEC 17025:2017版修订思路
ISO/IEC 17025:2017(以下简称“2017版”)基本继承了ISO/IEC 17025:2005(以下简称“2005版”)中的内容,只是对部分内容做了必要的更新、调整、补充。但从文件框架来看,却发生了很大变化,这是因为2017版的总体框架由ISO/CASCO(合格评定委员会)内部文件《QS-CAS-PROC/33公共要素》来决定。2017版中的注释也发生了变化,在此次修订中,尽量删除了2005版中的注和解释性的内容,有部分注释的内容经过修订后移入正文。例如2005版中5.4.5方法的确认中,5.4.5.2的注释3为当对已确认的非标准方法作某些改动时,应当将这些改动的影响制订成文件,适当时应当重新进行确认。而在2017版,这一内容成为正文——7.2.2.2当修改已确认过的方法时,应确定这些修改的影响。当发现影响原有的确认时,应重新进行方法确认。
2017版修订内容解读
由于ISO/IEC 17025:2017整个文件内容较多,课上张泽楷挑出了13个与2005版不同的地方进行解释,这样的对比学习,有助于高效掌握相关内容。
①文件(主体架构)变化
2005版的管理要求和技术要求在2017版中细分成通用要求、结构要求、资源管理、过程要求和管理体系5个部分。
②增加了9个术语
2017版出现了9个术语,其中对于“实验室”给出了明确的定义——从事下列一个或多个活动的机构:检测、校准或与后续检测或校准相关的抽样。而“独立的抽样活动”不再适用于实验室的概念。
③细化了公正性与保密性要求
关于公正性,2005版中的内容为4.1.5 :d.有政策和程序以避免卷入任何会降低其在能力、公正性、判断力或运作诚实性方面的可信度的活动。2017版中关于公正性的内容有以下4条:4.1.2 实验室管理层应做出公正性承诺;4.1.3 对实验室活动的公正性负责,不允许商业、财务或其他方面的压力损害公正性;4.1.4 实验室应持续识别影响公正性的风险;4.1.5 如果识别出公正性风险,实验室应能够证明如何消除或最大程度减小这种风险。
关于公正性,2005版中的内容为4.1.5 实验室应:c.有保护用户的机密信息和所有权的政策和程序,包括保护电子存储和传输结果的程序。2017版中关于保密性的内容有以下两条:4.2.1 实验室应通过做出具有法律效力的承诺,对在实验室活动中获得或产生的信息承担管理责任;4.2.4 人员,包括委员会委员、合同方、外部机构人员或代表实验室的个人,应对在实施实验室活动过程中所获得或产生的所有信息保密,法律要求除外。
④将“分包”与“服务和供应品的采购”合并
2005版中分别规定了检测和校准的分包与服务和供应品的采购,而2017版对于外部提供的产品和服务的观点为不论是采购产品,采购服务,还是分包,都是利用外部资源,所以可以合并成一个条款。
⑤增加了抽样记录要求
2005版中关于抽样记录的规定是记录应包括抽样程序、抽样人的识别、环境条件(如果相关)、必要时有抽样位置的图示或其他等效方法。2017版中对抽样记录的要求有所增加,其规定实验室应将抽样数据作为检测或校准工作的一部分并保留记录,增加的内容有抽样日期和时间、识别和描述样品的数据(如编号、数量和名称)、所用设备的识别、环境或运输条件,以及抽样方法和抽样计划的偏离或增减等。
⑥结果有效性的控制
2005版中对结果有效性控制的条款为“5.9 检测结果和校准结果质量的保证”,保证结果有效性的方法有:a.定期使用有证标准物质(参考物质)进行监控和/或使用次级标准物质(参考物质)开展内部质量控制;b.参加实验室间的比对或能力验证计划;c.使用相同或不同方法进行重复检测或校准;d.对存留物品进行再检测或再校准;e.分析一个物品不同特性结果的相关性。而2017版中对结果有效性的控制提出了更多建议,包括内部质量控制和外部质量控制。内部控制增添的内容有以下几点,使用其他已校准能够提供可溯源结果的仪器;测量和检测设备的功能核查;适用时,使用核查或工作标准,并制作控制图;测量设备的期间核查;实验室内比对;盲样测试等。外部质量控制的方法有能力验证和实验室间比对。
⑦报告结果内容的变化
报告结果是检验检测的重要部分,2017版中报告结果内容有如下变化。报告中不需要报告用户的地址,只需要报告用户的联络信息;增加了报告的发布日期;另外,需附有符合性声明。
⑧实验室的免责声明
2005版要求实验室未经书面批准不得复制(全文复制除外)检测报告或校准证书的声明。2017版中,除了2005版中不得复制报告的声明外,还要求做出免责声明。在如下两种情况实验室可以做出免责声明,一是对检测或校准物品的处置,当用户知道偏离了规定条件仍要求进行检测或校准时,实验室应在报告中做出免责声明,并指出偏离可能影响的结果。二是对于报告的通用要求,当用户提供的信息可能影响结果的有效性时,报告中应有免责声明。
⑨报告的符合性声明
实验室在报告符合性声明时应标识符合性声明适用于哪些结果;满足或不满足哪个规范、标准或其中哪些部分;应用的判定规则。要求实验室在实施2017版时,在合同评审阶段,实验室应将使用的判定规则与用户沟通,并在合同中予以明确,这样有利于报告的使用方了解实验室是如何做出符合性结论,以及实验室是如何考虑测量不确定度的,使结果更加科学。
⑩判定规则
2017版对“判定规则”进行了定义,即声明与规定要求的符合性时,描述如何考虑测量不确定度的规则。2017版增加了对“判定规则”的要求,也就是实验室在做与规范的符合性判断时,应该考虑测量的不确定度,特别是某些检测结果跨越了限值(超出限值)。所以实验室在做出“合格”或“不合格”的判断时,需要特别谨慎。
⑪管理体系的两种方式
2017版中管理体系可以用“两种方式”实施,一种是按8.2~8.9实施,另一种是按ISO 9001的要求建立并保持管理体系,但至少要包含从8.2~8.9的要素。
⑫引入风险管理
2017版引入了风险管理的概念,其中应对风险和机遇的措施参照了ISO 9001:2015。虽然2017版规定应该实施应对风险和机遇措施,但并未要求运用正式的风险管理方法,形成文件的风险管理过程。实验室是否有必要单独建立风险管理体系,由实验室自己决定。
⑬内部审核和管理评审的变化
2017版取消了内审周期的注释,规定实验室应按照策划的时间间隔进行内部审核,管理评审也应按照策划的时间间隔进行。对于管理评审,输入增加了以下要求:a.与实验室相关的内外部因素的变化;b.目标实现;k.实施改进的有效性;i.资源的充分性;m.风险识别的结果;n.保证结果有效性的输出(质控);o.其他相关因素,如监控活动和培训。输出增加了管理体系及其过程的有效性、履行本准则要求相关的实验室活动的改进、提供所需的资源和所需的变更等内容。
2017版特色
ISO/IEC 17025:2017的主要特色为文件的要素有所增加,由原来25个要素增加到29个要素。此外,在不降低要求的前提下,文件的要求更加灵活,使得实验室的自由度更大。2017版主要变化体现在报告的复合型声明、判定规则和风险管理方面。

相关热词搜索:关于ISO IEC 17025:2017的解读
[责任编辑:]

 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
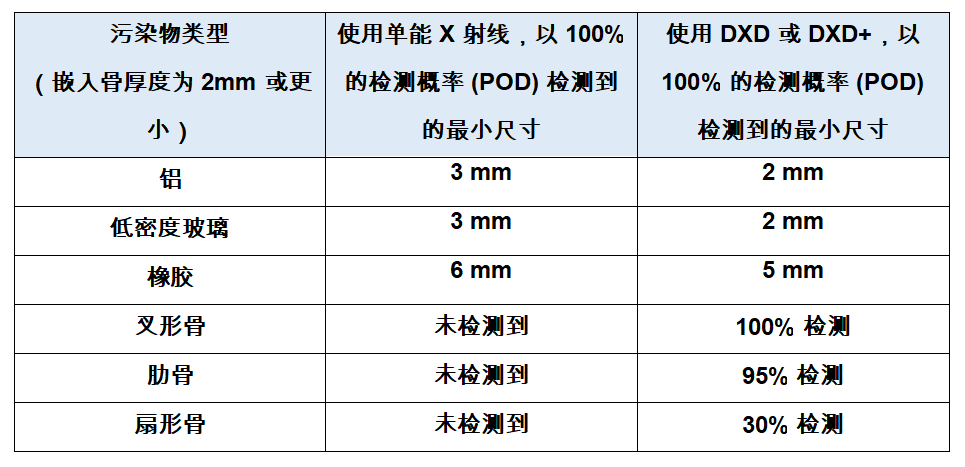 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!






参与评论