异源蛋白在丝状真菌中高效表达策略研究进展
在丝状真菌中实现高效表达的同源或异源蛋白很多,但是酶的高效表达与多个因素相关:宿主自身的特征,插入的外源基因或表达宿主自身的特征以及两者之间的不相容性或者相互影响而产生的一系列变化,使目的蛋白基因在表达宿主中很难实现高效表达。为了实现在丝状真菌中异源蛋白的高效表达,可以从两个方面来控制,一方面提高目的蛋白的表达量;另一方面抑制其它蛋白的分泌。其策略也可以从两方面来控制:一是外界条件,主要包括pH、温度、培养基等;二是基因的构建,主要包括使用高效强启动子、使用融合蛋白、使用转录因子、使用CCAAT图案的功能元件、构建蛋白酶缺陷株、增强基因拷贝数、构建高效的表达盒子、使用CRISPR/Cas9技术来编辑基因等。
外界条件的优化
不同的蛋白生长条件是不一样的,适应目的蛋白的条件不一定适应其它蛋白,那么可以通过改变外界的条件,间接地抑制其它蛋白的产生,从而促进目的蛋白的生长。不同的生长环境和不同的培养方法,都会影响异源蛋白的表达。菌体的生长反过来也会改变培养基的流动性,造成碳源、氮源、氧气和pH值等在发酵罐中分布不均。那么通过对接种量、碳源、氮源、发酵温度、转速、发酵时间以及pH的优化,可以提高目的蛋白的活力。
基因的构建
使用强启动子。经研究发现,为使丝状真菌能高效分泌异源蛋白,往往选用一些宿主自身的强启动子来进行调控。王兵兵成功构建了具有潮霉素B抗性标记的重组质粒pHB9,其中将来自黑曲霉的纤维二糖酶基因插入强启动子Pcbh1(包括分泌信号肽序列)和来自里氏木霉的Tcbh1终止子,从而提高蛋白的表达量。构建蛋白酶缺陷株。研究发现丝状真菌自身表达的蛋白酶能够明显影响异源蛋白的产量,那么可以根据这一特点,采取诱变或基因敲除等技术筛选出特异的蛋白酶缺陷的丝状真菌突变株,有的实验采用SMD1168蛋白酶缺陷性菌株,其Pep4基因突变,无蛋白水解酶活性,对表达的外源性蛋白产物降解极小,可明显提高蛋白表达量。增强基因拷贝数。引入多拷贝的表达载体,一般可以提高表达量。杨绍辉等人采用修饰信号肽,增加基因拷贝数的方法,实现高效表达。一般地说,目的基因整合到基因组中拷贝数越多,其转化子zeocin的抗性越强。因此,利用高浓度的zeocin平板可筛选到高拷贝数转化子,实现高效表达。使用转录因子。转录因子能控制基因的转录,可以调控RNA聚合酶与DNA模板的结合。通过表达转录因子hacA的活化形式可以实现黑曲霉中未折叠蛋白反应通路的组成型诱导,改善mRNA水平,从而提高外源蛋白的生产。使用CCAAT图案的功能元件。CCAAT图案被认为是真核生物中大量基因的高水平表达所必需的功能元件。它特异性结合蛋白激活物,然后引发一系列导致高水平基因表达的相互作用。通过将多个拷贝的含有CCAAT的蛋白质结合序列引入启动子来改善黑曲霉中的异源基因表达。构建高效的表达盒子。随着研究的不断进行,出现了以上传统的提高外源基因表达策略的两种相结合使用,出现了表达盒,有研究表明,使用组合型的强启动子以及增加异源基因的整合拷贝数的方法进行表达,但是其表达效果不是很好,其原因可能是在进行外源基因整合时,其整合的拷贝数是不确定的。所以说表达盒由于外源基因整合的随机性,使表达量的结果不太乐观。
CRISPR/Cas9技术。该技术是利用靶点特异性的RNA将Cas9核酸酶带到基因组上的具体靶点,从而对特定基因位点进行切割导致突变。使用该系统,内源基因组中的DNA序列及其功能输出可以在几乎任何选择的生物体中容易地编辑或调节。CRISPR/Cas9技术可以定向的敲除基因,敲除率几乎达到了100%,但是有的敲除率比较低,经研究表明载体构建时选择的启动子以及选择的策略不同,都会影响基因的敲除率,为了提高基因编辑效率最好选用同源强启动子。脱靶效应一直是该技术需要克服的重大技术问题。
随后,在一项新的研究中,韩春雨发现来自格氏嗜盐碱杆菌(Natronobacterium gregoryi)的一种Argonaute蛋白(NgAgo)作为一种核酸内切酶,在向导DNA(guide DNA,gDNA)的引导下,能够在人细胞中进行基因组编辑,通过设计进行大量的实验,发现NgAgo-gDNA具有广泛的基因组靶向范围和较低的错配耐受性,NgAgo能准确地将DNA片段插入到基因组中,与Cas9-sgRNA相比,NgAgo-gDNA具有更大的优势,规避了脱靶效应,其应用前景是不言而喻的。
问题分析
经研究发现,目前大多数还是使用传统的改造基因构造的策略,比如使用强启动子,增强基因的拷贝数,构建融合蛋白等,来提高异源蛋白的表达量,但是CRISPR/Cas9技术可以弥补传统方法上的不足,能更加准确地切割特定的位点,但是在查阅相关文献时,国内的大部分研究依旧是传统的高效表达策略,看不到与CRISPR/Cas9有关的内容。另一方面,虽然CRISPR/Cas9成为目前基因编辑最重要也最先进的技术,但是脱靶效应一直是它存在的主要问题,最近有人发现它可能会导致基因组不稳定性和破坏其他正常基因的功能,这将是CRISPR/Cas9系统应用于生物医学和临床应用的一个主要问题。
近年来,随着CRISPR/Cas9系统的改进和完善以及新的基因编辑工具的出现,使基因编辑更加简单,但是脱靶效应仍然存在,通过设计实验最大可能地提高目标活性,减少脱靶效应,从而实现更有效的遗传筛选和基因工程。有实验表明Cas9脱靶活性取决于sgRNA序列和实验条件,如John G.Doench就构建sgRNA活性的预测模型来发现改进活性的序列特征。这为减少脱靶效应提供了方向,此外,NgAgo-gDNA基因编辑系统的出现,可以预见未来的基因编辑发展的新方向,这将为基因定点突变、基因功能的挖掘、治疗医疗疾病模型的构建以及创制新的资源带来突破性的进展。
王春丽 朱凤妹 河北科技师范学院食品科技学院

[责任编辑:]

相关阅读
- (2018-08-01)粮油中真菌毒素检测技术及其应用
- (2016-06-24)转基因食品的营养学评价研究进展
- (2018-01-30)粮食中铅含量分析方法的研究进展
 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
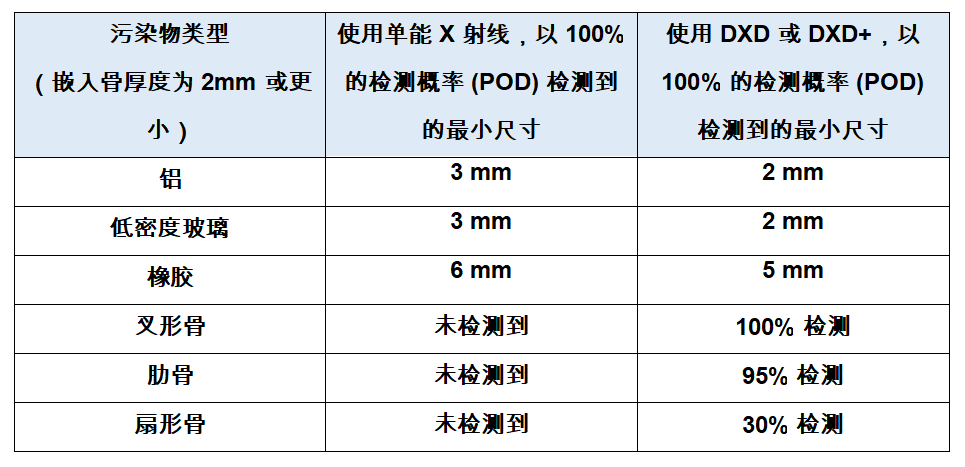 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!






参与评论