国内外李斯特菌检测及其快检技术的发展
摘 要:本文比较分析了国内外李斯特菌的检测方法、不同标准限量值的差异,并介绍了国内外李斯特菌快速检测技术的应用及存在的问题,对我国微生物快速检测的现状进行了概述,探讨了李斯特菌快速检测技术的未来发展方向,对李斯特菌检验方法探索及快速检测技术的发展具有一定的借鉴意义。
关键词:李斯特菌 快速检测 免疫学检测 分子学检测
李斯特菌广泛存在于环境中,并且在很多食品中有检出,该菌在低温的条件下仍能存活和增殖,其中单核细胞增生李斯特氏菌是食源性疾病的主要致病菌之一,也是食品安全控制的重要病原体,感染后会造成不同程度的人员死亡,受到各国的高度重视。传统方法检测费时费力而灵敏性较差,因此,快速、高效、灵敏可信的检测方法能够更加有效判定李斯特菌污染风险并且控制其危害。
1 李斯特菌的污染及危害
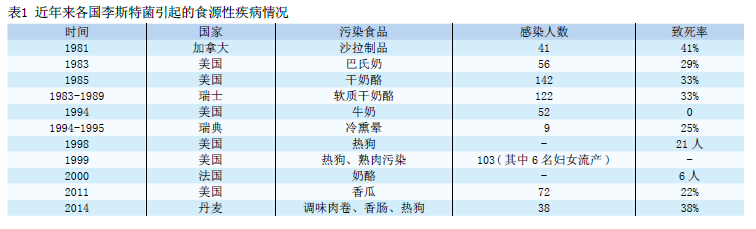
李斯特菌在环境中普遍存在,也是污染食品的主要病原菌,往往侵染肉类、蛋类、禽类、海产品、乳制品、蔬菜等食品,在4℃的环境中仍能生长繁殖,是冷藏食品中主要的病原菌之一。其中,单核细胞增生李斯特氏菌是食源性疾病的重要病原菌,WHO将其列为21世纪四大食源性致病菌之一[1]。近年来,单核细胞增生李斯特氏菌引起的食源性疾病事件时有发生(见表1),并造成不同程度的人员死亡,受到了各国的高度重视。
2 国内外关于食品中
李斯特菌限量的规定
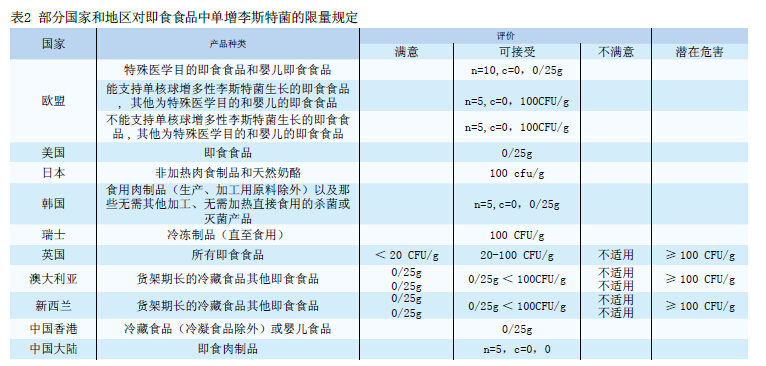
李斯特菌极容易污染食品,其中对冷藏食品和即食食品危害最为严重,各国均制定了食品中李斯特菌的限量值和监测计划。美国对即食食品中单增李斯特菌的限量规定为0/25g,并要求企业实施GHP和HACCP[2]。中国香港2014年修订了对即食食品和指定食品中单增李斯特菌的限量值并分别做了规定。冷藏食品(冷凝食品除外)或婴儿食品中单增李斯特菌必须“在25g食物样本中没有发现”,其他即食食品中单增李斯特菌的限量为食物样本中小于100CFU/g[3]。中国大陆2013年颁布的《食品中致病菌限量标准GB29921-2013》中规定[4],在即食肉制品中,单增李斯特菌按照二级采样方法取样不得检出(n=5,c=0,m=0)。也有一些国家,如新西兰等国家并没有制定相关的规定,仅制定了一个对人类健康不存在风险的可接受水平。综上,虽然各国均对单增李斯特菌做出了限量要求,但是对李斯特菌的限量各国的要求不一,见表2。
3 国内外主要检验方法
目前,食品微生物检测体系主要包括,中国的国家标准(GB4789)和检验检疫行业标准(SN)、国际化标准化组织(ISO)方法、美国食品药品监督局(FDA)、美国农业部(USDA)、美国官方分析化学师协会(AOAC)、加拿大健康保护部(MFLP)、欧盟食品安全局(EFSA)等检测体系[5]。
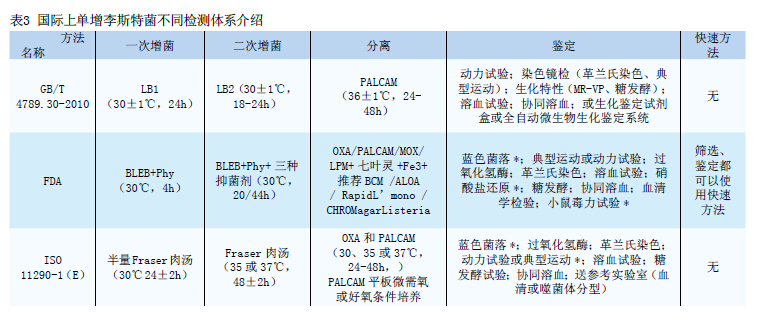
食品中单增李斯特菌的传统检测方法主要包括增菌、分离和鉴定3个环节[6]。目前,分离环节常会采用显色培养基,使其菌落颜色不同于其它干扰菌,实现快速分离。鉴定常采用生化反应和血清学反应。目前,生化反应的鉴定技术多采用数值分类鉴定和自动化检测技术。该技术主要包括:(1)API Listeria生化鉴定试纸条;(2)全自动微生物分析系统,如VITEK系统、MIDI系统及BIOLOG系统等。虽然该方法结果互认程度高,但操作强度大、检验周期长,需6~7d,无法实现快速检测。表3介绍了ISO、USDA、FDA、中国国标和行标等检测方法。
4 李斯特菌快速筛查技术
传统方法检测费时费力操作要求高,因此,李斯特菌快速检测技术和产品的开发是必要的。美国、欧盟等发达国家对微生物快速检测方法的研究和产品认证体系相对成熟,各种不同的快检系统和自动化仪器被推出,并得到广泛的应用。当前,李斯特菌快速检测方法为增菌以后,生化鉴定之前,对样本进行快速筛选,以缩小检测范围,减少检测任务,提高检测效率。快速检测方法主要包括酶底物显色技术、免疫学和分子生物学检测三大类。
4.1 即用培养技术
即用培养基技术则省掉了前期准备工作,可以直接检测样品,从而节约了大量人力成本。目前,商业化的固定培养基技术主要有两种:纸片法和即用平皿法。纸片法是指将显色培养基固定于纸片上,上方再盖一层带有方格的透明薄膜,以方便计数。即用平皿法是指用已倒有培养基的平皿,接种操作与传统涂板、划线法一样。其优点和纸片法一样,即省掉了前期准备工作,可以直接接种培养。
4.2 免疫学检测法
该技术以抗原抗体免疫为基础,制备特异性克隆抗体检测细菌。目前国内外李斯特菌快速检测的此类技术主要包括:酶联荧光分析法(ELFA)、金标免疫层析技术、流式细胞技术等。ELFA灵敏度比ELISA高,并省去了ELISA中的颜色反应,缩短反应时间;但缺点是成本较高,目前主要应用在自动酶联荧光免疫检测系统(VIDAS)上[7]。金标免疫层析技术是将高度特异性抗单增李斯特菌抗原的抗体束缚在色原载体上,且可与固相支撑基质相分离。当检测样品中存在李斯特菌时,测试单元的试剂将会被展开,产生肉眼可见的确定性反应。流式细胞术是一种在功能水平上对单细胞或其他生物粒子进行定量分析和分选的检测手段[6],它可以高速分析上万个细胞,并能同时从一个细胞中测得多个参数。
4.3 分子学检测方法
分子生物学检测方法主要包括核酸探针杂交技术、PCR检测技术等。DNA探针法是将两条碱基互补的DNA链在适当的条件下杂交,通过检测样品与标记性DNA探针之间形成的杂交分子来检测样品中的单增李斯特菌,测定放射性或荧光强度即可得出样品中单增李斯特菌的个数[8]。PCR是近年来广泛应用的分子生物学检测方法,在单增李斯特菌的检测中以其遗传物质高度保守的核酸序列(常用的靶序列包括hly、actA、prfA等)设计引物进行扩增。该方法特异性好,但灵敏度低,对样品进行前处理后再进行扩增,可以提高检出率和检测灵敏度。PCR技术还可对单增李斯特菌进行定量检测。国内外目前主要应用的PCR技术包括:实时荧光PCR(Real-time PCR)、多重PCR、恒温扩增、RT-PCR方法、IMS-PCR检测技术等[9]。
5 小结
微生物检测包括前处理、增菌、富集、检测等环节。为实现快速、实时、准确的监测食品微生物,每个环节都应有相应的筛查技术及产品。微生物快速检测今后的发展趋势主要是免疫学方法和核酸方法,分子检测技术具有高灵敏、高特异、快速等特点,在近几十年得到快速发展与应用,但相关技术还应向标准化、产品化方向发展,且开发更适合实时监测微生物的现场快速筛查技术与设备。免疫技术以高特异、快速特点而得到广泛应用。我国在微生物快速检测技术的应用及技术研发方面相对欧洲国家比较落后,快速检测技术的发展和应用需要政府相关机构、科研单位、企业共同的努力建立一套快速、准确、简单的检测体系,此外,还需要降低检测成本,提供检测灵敏度和实用性,这些是今后微生物快速检测的发展趋势。
参考文献
[1] Oevermann A,Zurbriggen A, Vandevelde M.Rhombencephalitiscaused by Listeria monocytogenes in humans andruminants: a zoonosis on the rise[J]. Interdisciplinary PerspectInfect on Infectious Diseases, 2010, 11(5): 142- 168.
[2] FAO/WHO.Food safety risk analysis-A guide for national food safety authorities[M].FAO Food and nutrition paper87.2006.
[3] 香港食品环境卫生署.香港食品微生物含量指引[S].2014.
[4] GB 29921-2013食品安全国家标准 食品中致病菌限量标准[S].2013.
[5] 何景,程楠,许文涛等.食品微生物新型快速筛查技术研究发展[J].食品科学,2014,10:1-8.
[6] 刘秀梅,杨洋,陈伟伟等.单核细胞增生李斯特氏菌检验(GB/T4789.30-2010)[S].北京:中国标准出版社,2012.
[7] 吕均,郑华英.PCR与mini-VIDAS 相结合快速检测食品中单增李斯特菌[J].中国卫生检验杂志,2010,20(7):1705-1706.
[8] 华晓芳,黄雪松.食品中单增李斯特菌的检测新技术[J].食品科技, 2007(6):230-232.
[9] 付瑞燕,周阳,祝长青等.食品中单增李斯特菌检测技术研究进展[J].安徽农业大学学报,2012,3(6):940-943.

[责任编辑:]

相关阅读
- (2014-09-05)沃尔玛试行食品安全检查新技术
- (2014-10-15)羊奶脱膻技术
- (2014-11-13)用技术筑牢食品安全防线
- (2014-12-08)Matrix模块化技术,推动西得乐稳步前行
- (2014-12-09)优势整合,以过硬的技术提供优质服务
 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
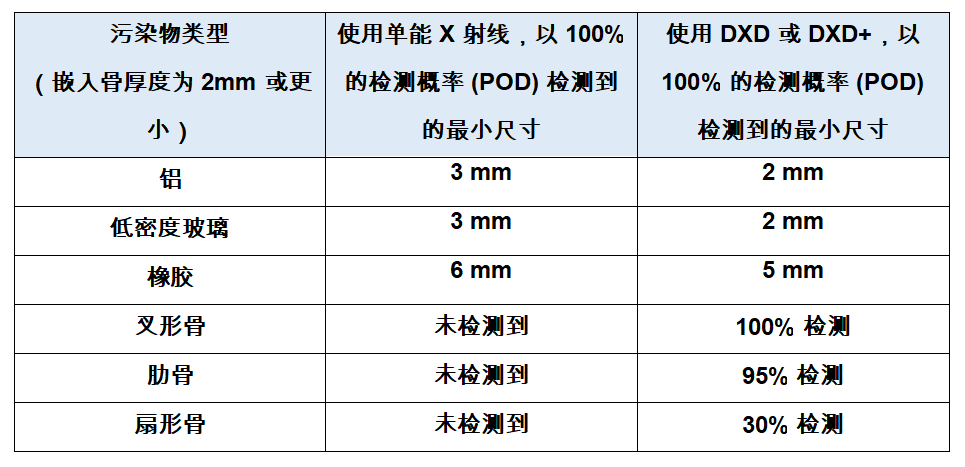 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!






参与评论